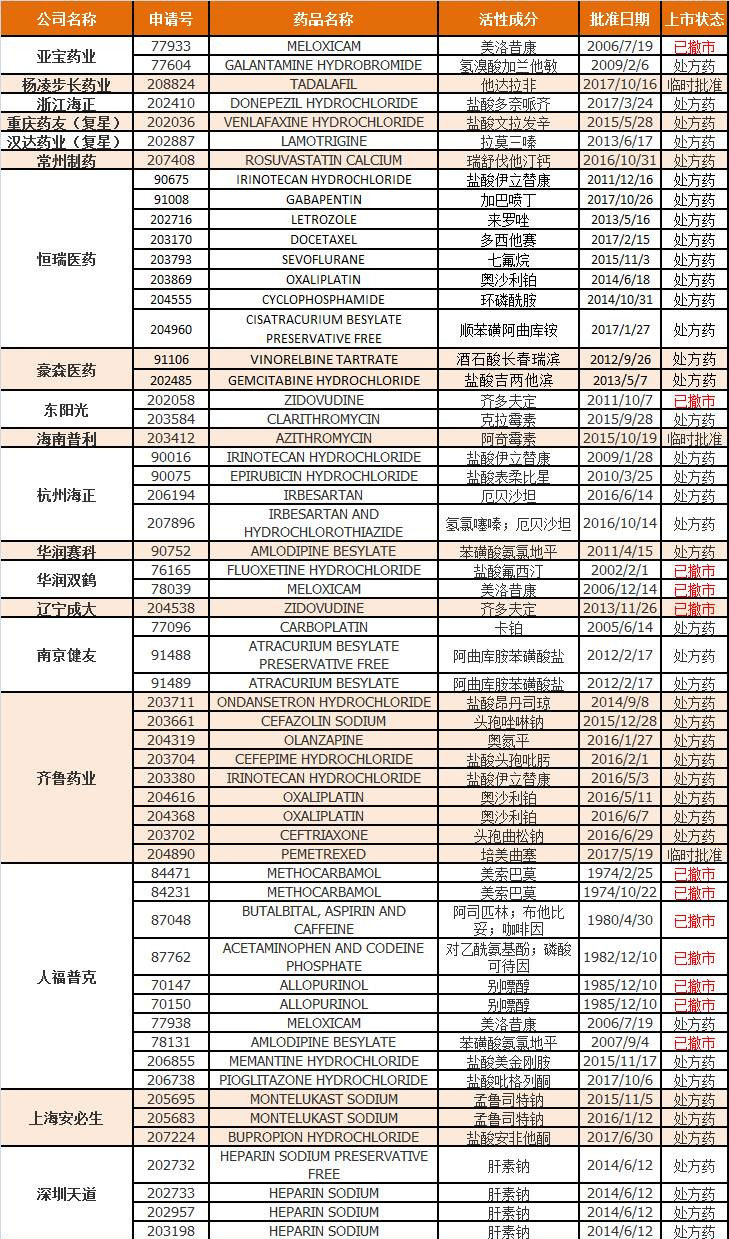
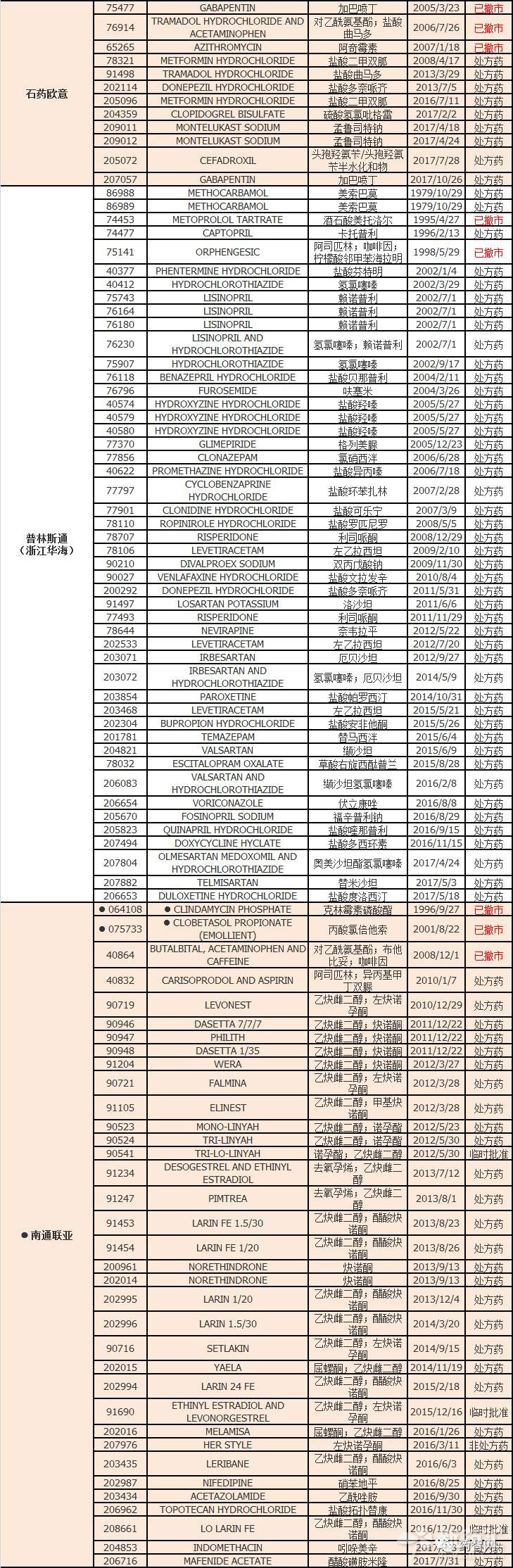
最新:2017年10月26日,石药欧意药业的加巴喷丁片获FDA批准,2017年10月16日杨凌步长制药有限公司的他达拉非片获FDA临时批准。
笔者通过药智美国FDA药品数据库对中国企业在FDA申报的ANDA药进行了不完全统计。数据显示,中国企业获得FDA批准的ANDA达到323个品规,152个申请号。浙江华海药业和南通联亚(品种相对单一,本文不作重点介绍)FDA申报数量遥遥领先。齐鲁药业、恒瑞药业、人福普克也持续发力,稳步进军美国市场。随着一致性评价的展开,仿制药获得美国或欧盟批准的可加速在我国报批审核的进程。另外,不少企业通过并购美国企业等作为进军海外市场的路径。如人福医药在2016以5.5亿美元收购美国Epic Pharma及附属企业,获得了Epic Pharma拥有的52个仿制药制剂文号(其中16个已撤市)。
以下是各中国企业ANDA获批数量统计,按申请号计(文章最后附中国药企获FDA批准的ANDA药详细表),如果不全,请您在后台留言。
企业名称 | 申报数量 |
普林斯通(浙江华海) | 48 |
南通联亚 | 35 |
石药欧意 | 12 |
人福普克 | 10 |
齐鲁药业 | 9 |
恒瑞医药 | 8 |
海正药业 | 5 |
深圳天道 | 4 |
上海安必生 | 3 |
南京健友 | 3 |
豪森药业 | 2 |
东阳光 | 2 |
华润双鹤 | 2 |
亚宝药业 | 2 |
华润赛科 | 1 |
汉达药业(复星) | 1 |
重庆药友(复星) | 1 |
辽宁成大 | 1 |
海南普利 | 1 |
常州制药 | 1 |
步长药业 | 1 |
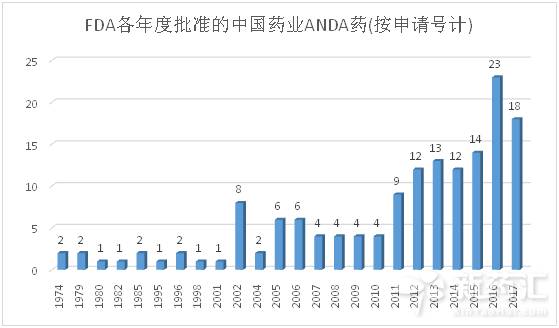
按年统计批准情况显示,FDA申报之路最早可追溯到1974年,人福普克药业可谓先驱者,最早申报了美索巴莫片(已撤市);5年之后的1979年,浙江华海也是通过申报美索巴莫开始了FDA申报之路。随着中国制药行业的发展,FDA批准的中国仿制药也不断增加,2016年达到了23个,其中齐鲁药业在2016年获得了6个ANDA制剂文号,常州制药在2016年首次获得了FDA批准的ANDA制剂。截止目前,2017年已经有18个申请号了,有望超过2016年。
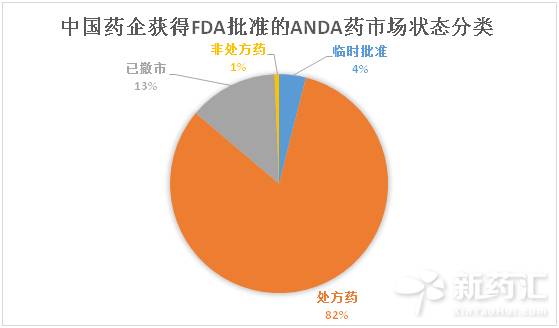
市场状态方面,处方药占了近82%的比例,也有13%的药品已经撤市了。值得一提的是由于专利权等原因,有6个药品获得的临时批准。
总体来说,中国药企的国际化道路正稳步前进。近年来,很多企业也获得了FDA的临床试验批准,希望中国药企能有真正NDA药上市。分析得比较粗浅,本次主要是给大家提供一个数据。更多信息可点击文末“阅读原文”访问药智美国FDA药品数据库,我们将在近期增加中国药企的检索项,敬请关注。